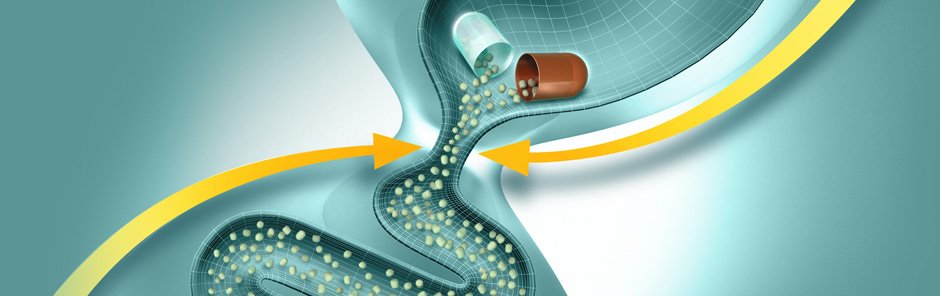
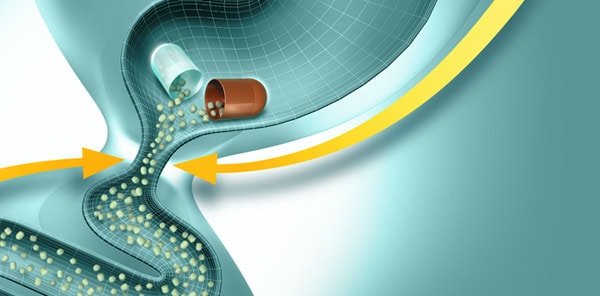
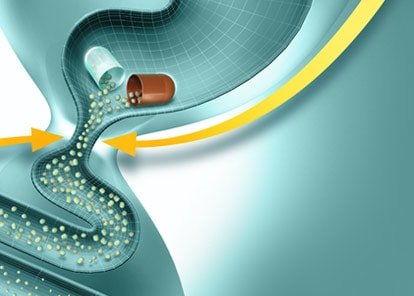
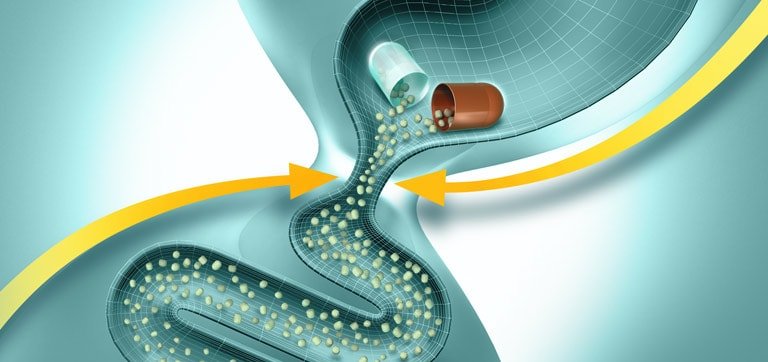
Клиникалық практикадағы панкреатиннің заманауи препараттары
И.В. Маев, Ю.А. Кучерявый
МБМ ЖКБ МММСУ Ішкі аурулар пропедевтикасы және гастроэнтерология кафедрасы
Полиферментті препараттар-бұл, негізгі әсер етуші субстраты таза түрдегі немесе қосымша компоненттермен (өт қышқылдары, гемицеллюлоза, симетикон, адсорбенттер және т.б.) біріктірілген панкреатин болып табылатын, аралас көп компонентті дәрілік заттар, негізінен жануар тектес.
Қазіргі уақытта фармакологиялық нарық құрамы мен клиникалық әсері бойынша әртүрлі полиферментті препараттарға өте бай, бұл олардың бірнеше түрлерін бөліп алу қажеттілігін анықтайды:
- Панкреатиннің таблеткаланған препараттары немесе өсімдік тектес ас қорыту ферменттері.
- Өт компоненттерін қосумен панкреатин препараттары.
- Құрамында адсорбенттер, симетикон, гемицеллюлаз және т. б. бар панкреатин препараттары немесе өсімдік тектес ас қорыту ферменттері.
- Құрамында панкреатиннің микросфералары/микротаблеткалары бар, энтеросолюбильді қабықпен қапталған капсулалар.
Ұйқы безінің ферменттерін тағайындау үшін басты немесе "академиялық" көрсеткіштер:
- экзокринді ұйқы безінің жеткіліксіздігін түзету;
- созылмалы панкреатит (СП) науқастарында ауырсынуды тоқтату;
- кез келген этиологиядағы қуыс ас қорытуының бұзылуы.
Мұндай көрсеткіштерді ас қорыту ферменттерінің қазіргі уақытта қолданылатын препараттарының көпшілігінің нұсқауларында табуға болады. Алайда, біз көріп отырғанымыздай, ферменттік препараттардың құрамы олардың құрамындағы ферменттердің мөлшері туралы айтпағанның өзінде айтарлықтай ерекшеленеді,ал көрсеткіштер қандай да бір дәрежеде ортақ болып табылады. Сонымен практикалық дәрігерге қандай препарат таңдау керек?
Мәселенің өзектілігі асқазан-ішек жолдарының барлық дерлік ауруларында кездесетін әртүрлі көрініс дәрежесіндегі ас қорыту үрдісінің бұзылуының төтенше таралуымен нығайтылады. Осылайша, симптоматикалық мақсатпен ұйқы безінің ферменттері көптеген гастроинтестиналдық симптомдарды персистирлеу кезінде, соның ішінде сау адамдарда да артық тамақтану, тамақтанудағы "қателіктер" кезінде қолданылуы мүмкін. Дегенмен, заманауи гастроэнтерологияның ең өзекті мәселесі созылмалы панкреатит (СП) болып табылады, өйткені:
- СП аурушаңдығы жылына 100 мың тұрғынға шаққанда 49,5–73,4 жағдай шегінде ауытқиды;
- соңғы 30 жылда әлемдегі жіті және созылмалы панкреатитпен ауыратын науқастар санының екі есе артуы байқалды;
- өлім-жітім 11,9%-ға жетеді.
Ұйқы безінің (ҰБ) сыртқы секреторлы жеткіліксіздігінің синдромы атрофия, фиброз, неоплазия нәтижесінде ҰБ жұмыс істейтін экзокринді паренхимасы массасының азаюымен немесе ҰБ шығыс жолдарының конкрементпен, ісікпен, қою және тұтқыр сөлмен бұғатталуы салдарынан ұйқы безі сөлінің аш ішекке (ОЕЕІ) кетуінің бұзылуымен байланысты. Сонымен қатар, ұйқы безінің ферменттері белсендірілмеген немесе ішекте әсерсіздендірілгенде қайталама ұйқы безінің жеткіліксіздігі делінетінді белгілеп өтеді.
ҰБ ферменттер секрециясының үлкен резервтік мүмкіндігіне ие, өйткені физиологиялық жағдайда ол тәулігіне, тағамды қалыпты қорытуға (физиологиялық гиперсекреция) қажет ететіннен 10 есе көп ферменттер мен зимогендерді қамтитын, екі литр ұйқы безінің шырынын шығарады. Демек, мальабсорбция синдромын дамыту үшін секреторлық мүмкіндік физиологиялық гиперсекреция көлемінің шамамен 5-10 % деңгейіне дейін айтарлықтай төмендеуі тиіс.
Бір қарағанда, ҰБ сыртқы секреторлық жеткіліксіздігі бар СП науқастарында пайда болатын мальабсорбция синдромын емдеу өте қарапайым болып көрінеді. Шынында да, экзогенді ұйқы безінің ферменттерін ауыстыру мақсатында қарапайым ауызша қабылдау өте тиімді болуы керек. Алайда, ұйқы безінің жеткіліксіздігінің клиникалық көріністерін толық түзетуге жиі қол жеткізілмейді, бұл көптеген түрлі факторларға байланысты, біз оның талдауың төменде көрсететін боламыз.
СП науқастарында ауру ұзақтығының ұлғаюына қарай ферменттердің секрециясы одан әрі азаяды, бұған қоса липазаның жетіспеушілігі үлкен дәрежеде байқалады және трипсин тапшылығына қарағанда бұрын дамиды. Бұл келесідей түсіндірілуі мүмкін:
- Липаза, амилазамен және протеаздармен салыстырғанда, протеолитикалық гидролизбен әсерсіздендіруге көп дәрежеде шалдығады.
- Ұйқы безінің протеаздарының жеткіліксіздігі ішек протеаздарымен және пептидаздармен, ұйқы безінің амилазаларының – сілекей мен ішектің амилазаларымен өтелуі мүмкін. Сілекей және асқазан липазасының басқа ұйқы безінің ферменттеріне қарағанда теңгеруші мүмкіндіктері айтарлықтай төмен және стеатореяның пайда болуын болдырмауы мүмкін емес.
- ҰБ экзокринді жеткіліксіздігінде ұйқы безінің ферменттерінің синтезінің төмендеуімен қатар бикарбонаттар секрециясының төмендеуі байқалады,бұл ОЕЕІ-тегі рН деңгейінің үдемелі құлдырауына әкеледі. 5,0-ден төмен рН кезінде липаза басқа ферменттерге қарағанда тезірек жойылады. Сонымен қатар, интрадуоденальді рН төмендеген кезде өт қышқылдарының преципитациясы төмендейді, мицеллдің қалыптасуы бұзылады, соның салдарынан қосымша май сіңуі бұзылады.
Жалпы алғанда, ҰБ экзокриндік жетіспеушілігінің клиникалық манифестациясы гастроинтестиналдық моториканың, асқазан, билиарлы және жіңішке-ішек секрециясының, абсорбцияның, гормондардың секрециясының және абдоминалдық хирургияның салдарларының (асқазан резекциясынан және гастрэктомия, холецистэктомия, билиодигестивті шунттау және т.б. кейінгі жағдай) ерекшеліктерін қамтитын қайталама факторларға байланысты. Жоғарыда көрсетілген бұзушылықтарды түзету бірқатар жағдайларда сыртқы секреторлық ұйқы безінің жетіспеушілігінің көріністерін азайтуға ғана емес, оны толық тоқтатуға да ықпал етуі мүмкін. Сондықтан көптеген авторлар ҰБ экзокриндік жеткіліксіздігін бастапқы және екіншілік деп бөлуді қалайды. Бұл СП науқастарында екіншілік ұйқы безінің жеткіліксіздігі ҰБ сақталған экзокриндік функциялары аясында да, сондай-ақ, оны одан сайын ушықтыра отырып, бастапқы сыртқы секреторлық жеткіліксіздік аясында дамуы мүмкін екедігін айта кеткен жөн.
Біздің ойымызша, мальдигестия және мальабсорбция синдромдары кезінде ас қорытуды қалыпқа келтіретін ең әмбебап құралдар асқазан, бауыр, билиарлық жүйе және ішек моторикасына әсер етпейтін панкреатин препараттары болып табылады. Бұл ферменттер ас қорыту белсенділігінің жеткілікті спектрін қамтамасыз етеді және жүрек айнуы, іштегі қорылдау, метеоризм, стеато-, креато - және амилорея сияқты клиникалық белгілерді тоқтатуға көмектеседі. Полиферментті кешенге кіретін амилаза өсімдік клетчаткасының гидролизіне қатыспай, көбінесе жасушадан тыс полисахаридтерді қарапайым қанттар - сахарозалар мен мальтоздарға дейін ыдыратады. Панкреатин препараттарындағы протеаздар негізінен химотрипсинмен және трипсинмен көрсетілген. Липаза бейтарап майдың гидролизіне қатысады.
Құрамдастырылған препараттар құрамында панкреатинмен бірге өт қышқылдары, гемицеллюлаза, симетикон, өсімдік тектес өт айдайтын заттарды және т. б. қамтиды. Препаратқа өт қышқылын енгізу оның ас қорыту безінің функциясына және асқазан-ішек жолының моторикасына әсерін айтарлықтай өзгертеді. Ұйқы безінің секрециясы мен тырысқақ артады, ішек және өт қабының моторикасы ынталандырылады. Ішектің микробтық контаминациясы жағдайында олардың деконъюгациясы болады, бұл кейбір жағдайларда осмотикалық және секреторлық іш өтудің дамуына ықпал етеді. Олар ҰБ секрециясын арттыратындықтан, ішектің перистальтикасын және өт қабының моторикасын ынталандыратындықтан, ішек ішілік осмотикалық қысымды, демек, ауырсыну абдоминальды синдромын, арттыратындықтан, құрамында өт қышқылдары бар ферментті препараттар СП ісінген және ауырсынатын нысандары бар науқастарға қарсы көрсетілетінін есте сақтау қажет.
Ұйқы безінің ферменттерімен алмастыру терапиясының негізгі мақсаты ОЕЕІ ішіндегі липазаның жеткілікті белсенділігін қамтамасыз ету болып табылады. Тұз қышқылының ұйқы бездік ферменттерге әсері олардың санының 90% - ға дейін бұзылуына әкелетіні белгілі, сондықтан, асқазанның қышқылдық барьерін жеңу арқылы, оларды қолдану қабықсыз панкреатиннің салыстырмалы мөлшерімен салыстырғанда майлардың сіңуін едәуір арттыратын [1], полиферментті препараттардың қышқылға төзімді қабықтағы галеникалық формаларын құру пайда болды.
Егер асқазандағы тамақтан кейінгі рН секрецияның жеке ерекшеліктеріне, сондай-ақ тамақ мөлшеріне және оның асқазанда болу уақытына байланысты болса, аш ішектің қуысында болатын (интрадуоденальды) рН ҰБ бикарбонаттарының қалдық секрециясына, аш ішектің бикарбонаттарының секрециясына, көлемнің сұйылуынан, сондай-ақ тұз және өт қышқылдарының мөлшеріне байланысты. Ұйқы безінің ферменттерінің қышқылға төзімді формаларын пайдалану екі маңызды жағдайды қояды – интрагастральды рН 5-тен аспауы тиіс, себебі бұл жағдайда ферменттер энтеросолюбильді қабықтан асқазанда босатылады, ал интрадуоденальды рН ОЕЕІ-те ферменттерді барабар босату үшін 5,5-тен төмен болмауы тиіс.
Тиімді алмастырушы ферменттік терапияны жүргізуді қиындататын маңызды фактор - ферменттік препараттар мен тағамдық түйірдің асинхронды гастродуоденалды қозғалысы болып табылады, ол пассаждың бұзылуы кезінде (қалтқы стенозы, ваготомиядан кейінгі жағдайы және т.б.), сондай-ақ ферменттік препараттарды салыстырмалы түрде үлкен мөлшерде қолданғанда байқалады.
Көптеген ферменттік препараттар ішекте еритін қабықтардағы драже немесе таблетка түрінде шығарылады, бұл ферменттерді асқазанда босатудан және асқазан сөлінің тұз қышқылынан бұзылудан қорғайды. Көптеген таблеткалардың немесе драженің өлшемі 10 мм және одан да көп болып келеді. Дегенмен, асқазаннан тамақпен бір мезгілде диаметрі 2 мм-ден аспайтын, оңтайлы мөлшерде 1,4 мм болатын қатты бөлшектер көшірілуі мүмкін екендігі белгілі [2]. Неғұрлым ірі бөлшектер, атап айтқанда, таблеткадағы немесе дражадағы ферменттік препараттар, ас химусы ОЕЕІ-те болмаған кезде тағам аралық кезеңде көшіріледі. Нәтижесінде препараттар тағаммен араласпайды және ас қорыту үрдісінде белсенді қатыспайды. Егер таблетка немесе драже ұзақ уақыт бойы асқазанда болса, энтеросолюбильді қабық бұзылады,ал ішіндегі ферменттер әсерсіздендіріледі.
Ұйқы безінің липазасының тамақтан кейінгі ең жоғары физиологиялық түсуі тамақтан кейін 4-6 сағат ішінде шамамен 140 000 ӘБ/сағ-ты құрайтындықтан [3], ал егер аш ішекке ферменттің қалыпты ең жоғары өнімінің 5% - дан астамы түссе, мальабсорбция дамымайтын болса, онда, стеатореяны түзету үшін тамақтан кейінгі кезеңнің 4-6 сағаты ішінде шамамен 28-42 000 ӘБ липазаның түсуін қамтамасыз ету қажет. Қазіргі уақытта, ішіндегі липаза құрамы айтарлықтай қатты өзгеретін (0-40 000 ӘБ шегінде), әртүрлі полиферментті препараттардың көп саны бар. Тиісінше, стеатореяны түзету үшін липазаның жоғары мөлшері бар препараттарды ғана пайдалану қажет. Алайда тәжірибеде ең жиі қолданылатындар, бір таблеткада (дражеде) 3 500-6 000 ӘБ шегінде липазасы бар "коммерциялық қолжетімді" препараттар болып табылады. Тиісінше, стеатореяны түзету үшін ең аз тиімді бір реттік мөлшер кем дегенде 5-8 драже немесе таблетка қабылдау болады. Алайда, бұл салыстырмалы есептеулер, өзінің көрсетімділігіне қарамастан, мұндай таблеткалардағы қолданылатын липазаның басым бөлігі препараттың толық емес фармакокинетикасына және химуспен бір мезгілде пассаждың мүмкін еместігіне байланысты әсерсіздендірілуі немесе белсендірілмеуі мүмкін екендігін ескермейді. Бұл жағдайда 5-8 таблетка туралы емес, дәлірек айтсақ - психологиялық себептер бойынша мүмкін емес, әрбір ас ішу үшін 20-30 таблетка туралы айту қажет. Осылайша, дәстүрлі қолданылатын экзогенді қабылданатын ферменттердің аз мөлшері, стеатореяны азайтатын болса да, неліктен оны ешқашан толығымен жоймайтыны түсінікті болады.
Сонымен, ферменттердің тағамдық химуспен тез және гомогенді араластырылуын қамтамасыз ету үшін, асқазан ішілік әсерсіздендірілуді болдырмау және асқазаннан ОЕЕІ-ке барабар пассажды қамтамасыз ету үшін диаметрі 1,8 мм аспайтын микротаблеткалар (Эрмиталь) түріндегі панкреатиннің жаңа буын ферменттік препараттары жасалды. Препарат энтеросолюбильді қабықпен жабылған және желатинді капсулаларға салынған. Асқазанға тиген кезде желатинді капсулалар тез ериді, микротаблеткалар тамақпен араласады және біртіндеп ОЕЕІ-ке түседі. Дуоденальды құрамның рН 5-тен жоғары болғанда қабықтар ериді және ферменттер үлкен бетте әрекет ете бастайды. Бұл ретте, ұйқы безінің шырыны асқазаннан тағамның мезгіл-мезгіл келіп түсуіне жауап ретінде бөлінген кезде ас қорытудың физиологиялық үрдістері іс жүзінде пайда болады.
Осылайша, микротаблеткаланатын препараттарды, , оның ішінде эксперименталды, теориялық, биохимиялық және клиникалық жұмыстар негізінде қалыптасқан осы препараттарға қойылатын заманауи талаптарға жауап беретін [4-6], алмастырушы ферментті терапияға арналған ең заманауи полиферментті препараттарға жатқызуға болады:
- препараттар жануар тектес болуы тиіс, негізінен шошқа тектес;
- ОЕЕІ қуысында нутриенттердің толық гидролизін қамтамасыз ететін ферменттердің жеткілікті мөлшерінің болуы (бір ас қабылдауға липазаның құрамы 36 000 ӘБ дейін);
- ферментті асқазан шырынымен қорытудан қорғайтын қабықтың болуы;
- тамақпен біркелкі және жылдам араластыру;
- ферменттердің ОЕЕІ-тегі қалтқы арқылы тамақпен бір мезгілдік пассажы;
- аш ішектің жоғарғы бөлігінде ферменттердің тез босатылуы;
- препарат құрамында өт қышқылдарының болмауы;
- қауіпсіздік, уыттылықтың болмауы.
Сондықтан, экзокринді жеткіліксіздігі бар СП-да бірінші таңдау препараттары ретінде Эрмиталь, Креон, Микразим және Панцитрат препараттарын санауға болады. Кең қолданылатын мезим форте препаратын тәулігіне 3-6 таблетканың мөлшерінде тамақтанудағы қателіктер кезінде пайда болатын ҰБ дисфункциясын түзету үшін ғана пайдалануға болады. Ал сол кезде белсенділігі 36 000 ӘБ, 40 000 ӘБ липаза препараттары ҰБ экзокринді функциясын толық алмастыра алады [7].
Полиферментті терапияның жанама әсері жиі емес және әдетте ауыр сипатқа ие болмайды. Осыған қатысты ең көрнекілері, сау еріктілерде 4 апта бойы липолитикалық белсенділіктің 360 000 (!) ӘБ тәуліктік мөлшерінде панкреатинді қабылдаған H.Friess және авторластардың зерттеулері болды. Авторлармен ҰБ экзо - және эндокриндік функциясының адаптациялық өзгерістері, оның өлшемдерінің өзгеруі табылған жоқ, сонымен қатар айтарлықтай жанама әсерлері байқалған жоқ [8], бұл тағы да панкреатин препараттарын айтарлықтай қауіпсіз деп сипаттайды.
Сыртқы секреторлы жеткіліксіздігі бар СП-да ферменттік препараттар өмір бойы тағайындалады, алайда, мөлшері көптеген факторларға байланысты өзгеруі мүмкін, соның ішінде науқастың диетаны сақтауына. Осылайша, ферментті препараттың мөлшерін таңдау туралы шешім әрбір науқас үшін жеке қабылдануы тиіс. Препараттың құрамына кіретін ферменттер белсенділігінің концентрациясын таңдау кезінде, құрамының төмендеуі ҰБ экзокриндік жеткіліксіздігінің айқын көрінуін көрсететін, фекальды эластаза белсенділігінің деректерін басшылыққа алуға болады деп есептейміз. Эластазды сынақ қазіргі уақытта ҰБ сыртқы секреторлық жеткіліксіздігін диагностикалаудың инвазивті емес әдістерінің ең ақпараттысы болып табылады және сонымен қатар ол кең қол жетімді болып келеді. СП науқастарында полиферментті препараттың мөлшерін таңдау әдістемесі қолданылған бірқатар зерттеулер мөлшерді бастапқы таңдау кезінде фекальді эластаза деңгейіне бағдарланудың клиникалық мақсаттылығын көрсетті [2]. Сыртқы секреторлық жетіспеушіліктің эластазды сынақ мәліметтері бойынша диагностикаланған деңгейге байланысты, дифференцияланған полиферментті терапия тағайындалады (кесте). Кестелік деректерге сәйкес, ҰБ қалыпты экзокринді функциясы бар СП науқастарына диспепсия симптомдарын түзету мақсатында, метеоризм және ауырсынатын абдоминальды синдром кезінде тәулігіне кемінде 50 000 ӘБ липазалық белсенділік мөлшерінде панкреатиннің қазіргі заманғы препараттарын курстық қабылдауды тағайындауға болады. Экзокриндік жеткіліксіздігі бар науқастарға полиферментті препараттардың біршама жоғары бастапқы мөлшерлері ұсынылады.
Сыртқысекреторлы жетіспеушілігі бар созылмалы панкреатитпен ауыратын науқастардың көпшілігі жиі бөлшек қоректендірудің ұсынымдарын ұстана отырып, диетаны сақтайды, оларда, әдетте, тағамның барлық тәсілдері бірдей және кестеде көрсетілген схема бойынша ферменттерді қабылдауға болады. Егер пациенттің диетасы дәстүрлі 3 тамақтану және 2-3 аралық тамақтардан тұрса, онда, ҰБ экзокриндік жетіспеушілігінің дәрежесіне байланысты негізгі тамақтануға липазаның 36 000 ӘБ дейін және аралық тамақтануға 10 000-20000 ӘБ қабылдау ұсынылады. Ең жоғары әсерге қол жеткізу үшін ферментті препараттар тағамның ең басында және мүмкіндігінше тамақтану кезінде фракциялы түрде қабылдануы тиіс (1 капсуладан артық қабылдағанда).
Клиникалық айқын көрінген ұйқы безінің жеткіліксіздігі кезінде әдетте препараттардың жоғары мөлшерлерінің көмегімен де стеатореяны толығымен жоюға болмайды, сондықтан ас қорыту ферменттерінің таңдалған мөлшерінің барабарлығының өлшемі дене салмағының артуы, нәжістің қалыпқа келуі (күніне 3 реттен аз), метеоризмнің азаюы болып табылады.
Алмастырушы ферменттік терапияның тиімсіздігінің себептері келесідей болуы мүмкін:
- панкреатогенді мальабсорбцияны еліктейтін немесе, ауыр экзокринді ұйқы безінің жеткіліксіздігін ауырлататын және ерекше емдеуді қажет ететін (глютенді энтеропатия, ішектің қабыну аурулары, тиреотоксикоз, ішек құрт инвазиялары, амебиаз, лямблиоз және т. б.), СП ілеспелі патологияның болуы;
- энтеросолюбильді қабықтағы (асинхронды гастродуоденалдық тасымалдау) панкреатиннің таблеткаланған препараттарын тағайындау;
- перистальтиканы күшейтетін және осмотикалық іш өтуді тудыратын, құрамында өт бар препараттарды тағайындау;
- емдеудің жалпы құнын төмендету үшін ферменттердің (оның ішінде микрокапсулаланған) барабар емес төмен мөлшерлерін тағайындау;
- комплаенстің бұзылуы (диетадағы бұзылулар, полиферментті препараттарды қабылдау мөлшерінің, уақыты мен еселігінің ерікті өзгеруі);
- ұйқы безінің қайталама жеткіліксіздігіне әкелетін ықтимал механизмдерді есепке алмау (ОЕЕІ ацидификациясы, артық бактериялық өсу синдромы, постгастрорезекциядан кейінгі бұзылулар және т.б.).
Шынында да, СП бар пациенттерде, алмастырушы полиферменттік терапияның тиімділігін төмендететін, артық бактериялық өсу синдромы жиі байқалады [9]. Сондықтан экзокринді жеткіліксіздікті барынша барабар емдеу үшін ішек микробиоценозының бұзылуын жоятын препараттардың емдік кешенінің құрамына міндетті түрде қосылуы қажет [10].
Осылайша, ұйқы безінің экзокринді жетіспеушілігін емдеу күрделі мәселе болып қалады, кешенді тәсілді талап етеді; консервативті емдеу схемасын таңдау кезінде экзокринді және трофологиялық жеткіліксіздік дәрежесін, ауырсыну абдоминальды синдромының және эндокриндік бұзылулардың айқындығын ескере отырып, әрбір жеке алынған жағдайда жеке тәсіл қажет. Соңғы жылдары әзірленген, протеаз бен липазаның олардың субстраттарына тікелей араласуы мен сегрегациясын айтарлықтай жақсартатын, ферменттік препараттардың галениялық нысандары, ұйқы безінің жеткіліксіздігі кезінде алмастыру терапиясының сапасын едәуір арттырады. Препаратты асқазандағы тұз қышқылынан қорғайтын қабықпен қапталған таблеткаланған полиферментті препараттарды қолдану іс жүзінде пайдасыз; тек энтеросолюбильді қабықпен қапталған панкреатиннің минимикросфералары бар соңғы ұрпақтың препараттары стеатореяны анық және мөлшерге тәуелді азайтады.
Созылмалы панкреатит кезіндегі ауырсынулы абдоминальды синдром осы аурудың ең типтік және жиі тіркелетін көрінісі болып табылады, ал ауруды тоқтату науқастарды емдеудің маңызды мәселесі болып табылады. АҚШ-та және Батыс Еуропаның бірқатар елдерінде ұйқы бездік ауруды басуға арналған бірінші желінің препараттары есірткіге жатпайтын анальгетиктер болып табылады. Бұл ретте, көптеген науқастарда анальгетиктермен ауырсынудың тиімді бәсеңдеуі ең жоғары рұқсат етілген тәуліктік мөлшерлерде ғана мүмкін. Теріс кері байланыс қағидасы бойынша ұйқы безінің секрециясын релизинг-пептидтермен реттеу механизмін ашу панкреатин препараттарын ауырсыну панкреатиттерді кешенді емдеу схемасына негізді қосуға әкелді. Алайда, қазіргі уақытта бар әдеби деректер мен осы мәселеге арналған сараптамалық пікірлер өте айқын және бір мәнді емес.
Өткен ғасырдың 70-ші жылдарынан бастап, ұйқы бездік протеаздардың ішкі жарық әсері ұйқы бездік секрецияны реттеуде маңызды рөл атқаратынын болжайтын бірнеше эксперименталдық зерттеулер жүргізілді [11, 12]. Ұйқы безінің секрециясын кері реттеудің негізгі тұжырымдамасы, ең алдымен, ОЕЕІ-тен ұйқы безінің сөлінің көшірілуі холецистокининнің (ХК) экспрессиясын және ұйқы безінің ферменттерінің секрециясын ынталандыратынын көрсеткен, эксперименталды жануарларға (егеуқұйрықтарға) жүргізілгензерттеулердің нәтижелеріне тірелді. Екінші жағынан, трипсинді немесе химотрипсинді аш ішек ішіне енгізу ХК экспрессиясын және ферменттердің ұйқы бездік секрециясын тежеді.
Кейінірек, қан плазмасындағы ХК деңгейінің артуы және ОЕЕІ-тен ұйқы бездік шырынды алып тастағаннан кейін ұйқы бездік секрецияның күшеюі, ішектің проксимальды бөлімдерімен секреттелетін және кейіннен холецистокинин-релизинг фактор деп аталған, трипсин-сезімтал субстратпен байланысты болғаны дәлелденді. Трипсиннің қатысуы кезінде ХК-релизинг фактор пептид бола отырып, бұзылады және осылайша, әсерсіздендіріледі. Аш ішекте тағам ақуызы трипсинді байланыстырады, шартты түрде ХК-релизинг факторымен фермент үшін бәсекелеседі, және тек трипсин артығы ғана ХК-релизинг факторды әсерсіздендіре алады. ХК релизинг факторының концентрациясының артуы аш ішектің саңылауында өз кезегінде ұйқы бездік секрецияны ынталандыратын ХК экспрессиясын тудырады (сурет. 1).
Адамда кері байланыстың осындай механизмі алғаш рет 1977 жылы сипатталған [13]. Шынында да, болашақта зерттеушілердің бірнеше тобы трипсинді немесе химотрипсинді ішке енгізу ҰБ ферменттерінің секрециясын тежейтінін растады [14-17]. Осылайша, СП бар пациенттерде сыртқы секреторлық жеткіліксіздік кезінде ұйқы бездік ферменттердің секрециясы қан плазмасындағы жоғары ХК деңгейлеріндегі ҰБ гиперстимуляциясына және демек, ауырсыну абдоминалдық синдромның пайда болуына немесе ушығуына әкелуі мүмкін екендігі көңілге қонымды болып көрінеді.
Кері байланыс механизмін ашу G.Isakson және I. Ihse үшін 80-ші жылдардың басында кері байланыстың дуоденопанкреатиялық механизмі арқылы СП кезіндегі ауырсынуды азайту үшін жоғары протеолитикалық белсенділігі бар полиферментті препараттарды қолдануды негіздеуге мүмкіндік берді [18] (сурет. 2). Жүргізілген қосарланған соқыр плацебо бақыланатын айқас зерттеудің мәліметтері бойынша авторлар қабықпен қапталмаған панкреатин таблеткаларын қабылдау аясында СП науқастарында ауырсыну абдоминалды синдромының айқын көрінуінің 30% төмендегенін және науқастардың көпшілігінде ауырсыну ұстамаларының санының төмендегенін хабарлады [18]. Алайда, бұл тәсіл ұйқы безінің қалыпты жеткіліксіздігі бар пациенттерде ғана тиімді болды.
- Slaff және авторластар өздерінің қосарланған соқыр плацебо бақыланатын тоғыспалы зерттеуінің шеңберінде СП ауырсыну формасы бар 20 пациенттерді бақылады [17]. Полиферментті препараттарды қабылдау аясында ауырсыну абдоминальды синдромының көрінуінің азаюы ҰБ жеңіл және орташа айқын экзокринді жеткіліксіздігі бар тоғыз пациентте байқалды, ал ұқсас әсері ҰБ ауыр сыртқы секреторлы жеткіліксіздігі бар 11 Науқастан 2-де ғана байқалады.
Жоғарыда келтірілген екі зерттеуде ферменттермен емдеуге жауап берген науқастардың көпшілігі идиопатиялық СП бар әйелдер болды, ал алкогольді СП бар ер адамдар көбінесе резистентті болып шықты. Алкогольді СП панкреатиттің (тұқым қуалаушылықты қоспағанда) басқа этиологиялық түрлеріне қарағанда, ҰБ ағындық жүйесінде ақуыз тығындарының (ерте кезеңде) және конкременттердің (кеш кезеңде) пайда болуымен сүйемелденетіні белгілі. Айқын вирсунголитиаз ҰБ ағындық жүйенің дилатациясымен және қарқынды ұйқы бездік ауырсынумен ілесіп жүреді. Мұндай науқастарда ферменттермен монотерапия кезінде ауырсыну синдромын тоқтату мүмкін емес, бұл панкреатиннің көбінесе әйелдердегі тиімділігі фактілерін түсіндіреді.
Бақыланатын зерттеу шеңберінде СП ауырсыну түрімен ауыратын науқастарда ферменттерді тағайындау кезіндегі жақсы әсер D.Ramo және авторластармен көрсетілді [20]. Жалпы, жоғарыда келтірілген үш қос соқыр зерттеулердің нәтижелері өте жағымды болып шықты, СП ауырсыну түрімен ауыратын науқастарда полиферментті препараттарды қолданудың жақсы нәтижесі 73% - ға жетті (49 бақыланатын пациенттің 36-ында) [17, 18-20]. Жоғарыда келтірілген барлық зерттеулерде қышқылдан қорғайтын қабықсыз панкреатин (котазим, виоказа) қолданылғанын атап өту қажет.
Қос соқыр 4 апталық айқас плацебо-бақыланатын зерттеуде панкреазаның екі капсуласын (энтеросолюбильді микротаблеткалар) әрбір тамақтану кезінде ішу арқылы тағайындау плацебо әсерімен салыстырғанда СП науқастарындағы ауырсыну абдоминальды синдромның айқын көрінуін азайтты [21]. Басқа мульти орталықты 2-апталық плацебо-бақыланатын зерттеуде, тамақтану кезінде ішекте еритін қабықтағы полиферментті препараттарды қабылдау СП науқастарындағы ауырсыну абдоминальды синдромның айқын көрінуіне әсер етпейтіні көрсетілген [22]. 4 айлық қос соқыр плацебо-бақыланатын айқас зерттеуде бұрын пайдаланылған микросфераларға (pH> 6) қарағанда PH (>5) төмен мәндерінде белсендірілетін ішекте еритін микротаблеткалар қолданылды. Авторларға препараттың фармакокинетикасының өзгеруі ОЕЕІ-те трипсиннің жоғары деңгейіне жетуге әкелгенін дәлелдеу қолдарына келді, бірақ ұйқы бездік ауырсынуды тежеудің сенімді динамикасы авторлармен байқалмады [23]. Сонымен қатар, жоғарыда келтірілген зерттеулерде [21-23] науқастардың когорттарында алдыңғы бақыланатын зерттеулерде ферментті препараттармен емдеуге ең жоғары дәрежеде жауап беретін әйелдердің аздаған саны қосылғанын атап өтпеуге болмайды. Бұдан басқа, осы зерттеулерге енгізілген пациенттердің басым бөлігінде басқа да ауырсыну патомеханизмдері (вирсунголитиаз, жалған сарысулы ісік және т.б.) бар, қарқынды ауырсыну абдоминалды синдромы тән, алкогольдік СП болды. Осылайша, жүргізілген бақыланатын зерттеулерді талдаудан кейінгі ең маңызды қорытынды ретінде PH (> 5) салыстырмалы түрде төмен мәндерінде белсендірілетін ішекте еритін микротаблеткаларды пайдалану кезінде ОЕЕІ-тің саңылауында протеаздардың жоғары концентрациясына қол жеткізу мүмкіндігі фактісін атауға болады.
Сонымен, соңғы уақытта СП науқастарында ауырсынуды тоқтату үшін панкреатиннің асқазанда және ОЕЕІ-тің (котазим, виоказа) жоғарғы бөлімдерінде белсендірілетін қышқылдан қорғайтын қабығы жоқ таблеткаланған препараттарын қолдану ұсынылатыны туралы пікір бекітілді [17, 18, 21-23]. Панкреатинді тұз қышқылынан қорғау үшін бұл препараттарды асқазан секрециясының блокаторларымен бірге қабылдау қажет. Бұл ретте панкреатиннің энтеросолюбильді емес таблеткалық препараттары Ресейде фармакологиялық нарықта ұсынылмайтынын және сондықтан қол жетімсіз, ал асқазан секрециясының блокаторлары, әсіресе протонды сорғы тежегіштері ұйқы бездік секрецияны ынталандырудың баламалы механизмін бұғаттау есебінен СП кезінде ауыр абдоминальды синдромды тиімді азайтатынын (ОЕЕІ ацидификациясы редукциясы есебінен ҰБ секреторлық кернеуінің азаюы) айта кету қажет [24].
Осылайша, егер дәлелді медицина ұстанымдарына сүйенетін болсақ, онда Ресейде тәжірибеден өтуші дәрігерлер маңызды таңдау алдында қалады – тиімділігі бақыланатын зерттеулерде мүлдем дәлелденбеген панкреатиннің таблеткаланған энтеросолюбильді препараттарын тағайындау немесе, олардың тиімділігі бақыланатын зерттеулерде біркелкі емес болған, микрокапсулаланған (микротаблеткаланған) заманауи полиферментті препараттарды тағайындау, бұл белгілі бір шамада дизайн ерекшеліктерімен түсіндіріледі.
Егер, бөлшектер мөлшерінің асқазаннан, әсіресе тамақпен бір мезгілде көшіру жылдамдығына тәуелділігін көрсеткен, тәжірибелік зерттеулерге сүйенетін болсақ, онда – ірі таблеткалар (диаметрі 2-3 мм артық) пилориялық арна арқылы баяу өтетіні анық болады. Олардың басым бөлігі бұзылады және тек фрагменттер түрінде ОЕЕІ-ке өтеді. Ірі мөлшердегі таблеткаларды жабатын энтеросолюбильді қабық таблеткалардың асқазанда болуын одан да кідіртеді, өйткені таблеткаларды фрагменттеу тек рН 5-тен жоғары, ал жиі 6 болғанда ғана мүмкін. Бұл жағдайда таблеткалар мен тамақты бір мезгілде көшіру туралы айтуға тура келмейді; таблеткалардың асқазанда кешіктірілуі, кейіннен оларды фрагменттеу препараттың 80% - ға жететін компоненттерінің әсерсіздендірілуіне ықпал етеді.
Осылайша, Ресейде қабықпен қапталмаған панкреатин препараттарының болмауы, СП кезінде ауырсынуды басуда таблеткаланған энтеросолюбильді препараттардың тиімділігінің дәлелді базасының болмауы, адам физиологиясының ерекшеліктерін есепке ала отырып, оларды қолданудың мақсатқа сай болмауы тәжірибелеуші дәрігердің алдына маңызды сұрақ қояды – ұйқы бездік аурулары бар науқастарға не тағайындау керек? Дәрігер-тәжірибелеуші аузынан қисынды шығатын тағы бір заңды мәселе – егер біз практикалық жұмыста эффектіні көріп отырсақ, панкреатин таблеткаларын қолданудың тиімсіздігі мен орынсыздығы туралы қалай айтуға болады?
Бірінші сұраққа жауап өз – өзінен сұралады – егер біз XXI ғасырда дәлелді медицинаға бағытталатын болсақ, онда біз бақыланатын зерттеулерде кем дегенде ішінара тиімділікті көрсеткен препараттарды қолдануға міндеттіміз -яғни 4 буындағы ферментті препараттар (микротаблеткалар, микросфералар), өйткені Ресейде энтеросолюбильді емес таблеткаланған препараттар қол жетімді емес. Бұл ретте, біз қабығы рН (шамамен 5) қышқыл мәндерінде еритін препаратты пайдалануға тиіспіз, бұл ОЕЕІ проксимальды бөлімдерінде трипсинді ерте белсендіруді және релизинг-пептидтерді инактивациялауды жүзеге асыруға мүмкіндік береді. Препаратты таңдаудың басқа талабы препараттағы протеаздың жоғары мөлшері болуы мүмкін.
Екінші сұраққа келсек, дәрігердің жеке тәжірибесі бақыланатын зерттеулермен салыстырғанда әлсіз дәлел болып табылады (дәлелді медицинаның 5 және 2 деңгейі тиісінше). Сонымен қатар, Ресейде мұндай науқастарды дәстүрлі жүргізу миотропты спазмолитиктерді, антисекреторлық, анестезиялық және т.б. препараттарды қосымша пайдалануды қамтиды. Панкреатиттің ауыр түрімен ауыратын және монотерапия ферменттерімен ауыратын науқастар іс жүзінде жоқ. Кешенді емдеуде панкреатин таблеткаларының әсерін қалай бағалауға болады?
Әрине, бізде энтеросолюбильді таблеткалардың ауырсынуды тоқтату тиімділігін көрсететін дәлелдер деңгейі бойынша бәсекеге қабілетсіз қарапайым салыстырмалы және сипаттама зерттеулерінің белгілі бір саны бар. Ас қорыту физиологиясы және энтеросолюбильді таблеткалардың фармакокинетикасы жағынан бұл препараттар асқазанда ұзақ уақыт бойы белсенді компоненттердің ішінара (80% - ға дейін) әсерсіздендірілу нәтижесінде ОЕЕІ-ке ас қорытудан тыс фазаға түседі. Онда трипсин релизинг-пептидтерді жойып, ҰБ ас қорыту аралық секрециясын азайтуға қабілетті. ҰБ секреторлық кернеуінің постпрандиальды күшеюіне және СП науқастарында ас ішкеннен кейін ауырсынудың классикалық күшеюіне энтеросолюбильді қабықпен қапталған панкреатин таблеткалары әсер ете алмайды. Энтеросолюбильді қабықпен қапталған таблеткалардың асқазанда болу ұзақтығы белгілі емес. Мүмкін, жиі бөлшек тамақтанудың ұсынымдарын ұстанатын бірқатар науқастарда олардың фрагменттеу және көшіру кезеңі тағамның арасындағы аралыққа тең болуы мүмкін. Басқаша айтқанда, таңғы ас кезінде қабылданған таблеткалардан панкреатин ОЕЕІ-ке тек бесіндік алдында ғана түседі. Бұл гипотезаның әзірге дәлелді базасы жоқ, алайда жанама растау бар.
Мысалы, жақындағы зерттеуде, дәстүрлі қабылдаумен салыстырғанда ауырсынуды тоқтатуға қатысты жақсы әсермен, тамаққа дейін 20 минут бұрын микрокапсулаланған панкреатин қолданылды (тамақ кезінде емес!)[25]. СП патофизиологиясына және, энтеросолюбильді қабықшасының бұзылуы рН 6 кезінде орын алатын, препараттың фармакокинетикасына сүйене отырып, тамаққа дейін қабылданатын панкреатин ОЕЕІ проксимальды бөлімдеріне постпрандиальды қышқылдық түсірудің басталуына дейін, яғни рН бейтарап мәніне жақын жерде ішінара түсуге үлгереді. Бұл минимикросфераның энтеросолюбильді қабықшаларының бұзылуына, ОЕЕІ прокисмальды бөлігінде трипсиннің белсендірілуіне және релизинг-пептидтердің бұзылуына ықпал етеді.
Жоғарыда айтылғандарды ескере отырып, Ресей нарығында бар барлық полиферментті препараттарға қатысты бірқатар маңызды артықшылықтарды сипаттайтын Эрмиталь 25 000 препаратына жеткіліксіз көңіл бөлінетіні біршама таңдандырады:
- микротаблеткалардың энтеросолюбильді қабықшаларының ашылуына әкелетін және трипсиннің ерте белсендірілуін (ОЕЕІ терминалдық бөлімінде) қамтамасыз ететін рН ең төменгі шекті деңгейі ;
- протеаздың ең жоғары құрамы (1 250 ӘБ).
Шынында да, Креон препаратында ферменттерді босату үшін рН оптимумы 6,0-ді құрайды; Эрмиталь препараты үшін – 5,0 [19], бұл, сірә, микросфералар мен микротаблеткалардың энтеросолюбильді қабықшаларының әртүрлі қасиеттерімен байланысты. Эрмиталь препаратын қабылдау препараттың құрамында онсыз да көп мөлшерде болатын ОЕЕІ бастапқы бөліміндегі протеаздың ерте белсендірілуіне әкеледі. Осылайша, Эрмиталь препаратын пайдалану рН-ның үлкен ауқымына байланысты болжанып отыруы мүмкін, оның шегінде препараттың жоғары белсенділігі және протеаздың жоғары мөлшері белгіленеді.
Соңғы жылдардағы зерттеулер СП кезіндегі ауыр абдоминалды синдромды емдеуде протеаздың жоғары құрамы бар панкреатиннің энтеросолюбильді препараттарының жоғары тиімділігін көрсетті. Осылайша, В. Т. Ивашкин мен авторластардың мәліметтері бойынша СП науқастарында энтеросолюбильді қабықта микротаблеткаланған панкреатинді қабылдау абдоминальды синдромның дұрыс тоқтауына алып келді, сонымен қатар жүргізілген факторлық талдау нәтижелері бойынша ауырсынудың азаю дәрежесі ҰБ экзокринді функциясының бәсеңдеу дәрежесіне байланысты болды [26]. Бұл авторлармен келесідей түсіндіріледі. Біріншіден, абдоминальды ауырсынудың генезі белгілі бір дәрежеде ішектің дискинетикалық бұзылуының болуымен және сіңірудің екінші рет бұзылуынан пайда болған метеоризммен байланысты. Екіншіден, панкреатиннің энтеросолюбильді формасын қолдану арқылы терапия аясында нәжістің эластазасы деңгейінің дұрыс төмендеуі панкреатиннің ауырсынуға қарсы әсері панкреатиннің ұйқы бездік секрециясын бәсеңдетумен байланысты болды деп санауға барлық негіз береді [26].
Қорытындыда, этиологиялық фактор, жынысы, ағымы ауырлығы және ҰБ экзокриндік жеткіліксіздігінің дәрежесі бойынша нақты рандомизацияланған СП науқастарының топтарында әртүрлі ферменттік препараттарды қолдануға арналған ұзақ мерзімді салыстырмалы зерттеулер перспективалы болып табылатынын атап өту қажет. Алайда, мұндай зерттеулердің болмауы, әрине, ауыр абдоминальды синдромы бар СП науқастарында полиферментті препараттармен ұзақ уақыт емдеу клиникалық және этикалық пайымдаулар бойынша мүмкін еместігіне байланысты. Біздің ойымызша, хирургиялық немесе эндоскопиялық емдеуге көрсетімдер болмаған кезде СП кезінде ұзақ уақыт сақталатын ауырсыну абдоминалдық синдромы біріктірілген емді пайдалану көрсеткіші болып табылады. Бұл көзқарас кез келген препараттармен монотерапияның белгілі бір тиімділігі аздығына да, СП кезінде абдоминальды ауырудың көпкомпонентті патомеханизм фактісіне де негізделеді. Патогенездің бірнеше буындарына бірден бір мезгілде әсер ету ғана табысқа әкелуі мүмкін.
Қышқылға төзімділікті, химуспен жылдам және бір мезгілде пилоро-дуоденальды транзитті, жылдам белсендіруді, протеаздың жоғары құрамын қамтитын едәуір заманауи препараттарды қолдану, табысты емдеудің және науқастардың өмір сүру сапасын жақсартудың кепілі болып табылады. Ұйқы бездік ауырсыну кезінде Эрмиталь препаратын қолдану пайдасына қосымша дәлел келесідей болуы керек. Ауырсыну абдоминалды синдромынан зардап шегетін СП науқастарының басым көпшілігінде орынбасушы ферменттік терапияны жүргізуді талап ететін бастапқы немесе қайталама экзокринді ұйқы бездік жеткіліксіздігі бар. Осы уақытқа дейін жарияланған барлық жүргізілген зерттеулермен ұйқы бездік жеткіліксіздікті емдеу кезінде ең тиімділікпен 4 буын препараттары ғана сипатталатыны дәлелденді, бұл елеулі дәрежеде СП екі маңызды синдромдарын – экзокриндік ұйқы бездік жеткіліксіздікті және ауырсыну абдоминалдық синдромды тоқтату үшін осы препаратты пайдаланудың орындылығын анықтайды.
Әдебиет
- Lankisch P.G., Buchler M., Mossner J. A primer of pancreatitis. Berlin: Springer-Verlag, 1997.
- Meyer J.H., Elashoff J., Porter-Fink V. et al. Human postprandial gastric empting of 1-3 millimeter spheres // Gastroenterology. 1988; 94: 1315–1325.
- DiMagno E.P., Go V.L.W., Summerskill W.H.J. Relationship between pancreatic enzyme output and malabsorption in severe pancreatic insufficiency // N. Engl. J. Med. 1973; 288: 813–815.
- Белоусова Е.А., Златкина А.Р., Морозова Н.А., Тишкина Н.Н. Гастроэнтерологияда ферментті препараттарды қолданудың ескі және жаңа аспектілері // Фарматека. 2003; 7: 39–44.
- Маев И.В., Кучерявый Ю.А. Гастроэнтерологиялық практикадағы полиферментті препараттар // Врач. 2003; 10: 59–61.
- Охлобыстин А.В. Гастроэнтерологияда ас қорыту ферменттері препараттарын қолдану // Клин. перспект. гастроэнтерол., гепатол. 2001; 2: 34–38.
- Щербаков П.Л. Ұйқы безі аурулары кезіндегі ферментті препараттар // Клин. мед. 2001; 11: 71–74.
- Friess H., Kleeff J., Malfertheiner P. et al. Influence of high-dose pancreatic enzyme treatment on pancreatic function in healthy volunteers // Int. J. Pancreatol. 1998; 23: 2: 115–123.
- Madsen J.L., Graff J., Philipsen E.K. et al. Bile acid malabsorption or disturbed intestinal permeability in patients treated with enzyme substitution for exocrine pancreatic insufficiency is not caused by bacterial overgrowth // Pancreas. 2003; 26: 2: 130–133.
- Старостин Б.Д. Созылмалы панкреатиттің аралас терапиясы (қос соқыр плацебо-бақыланатын сынамалы зерттеу)// Эксп. и клин. гастроэнтерол. 2003; 3: 58–65.
- Green G.M., Lyman R.L. Feedback regulation of pancreatic enzyme secretion as a mechanism for trypsin inhibitor-induced hypersecretion in rats // Proc. Soc. Exp. Biol. Med. 1972; 140: 6.
- Louie D.S., May D., Miller P. et al. Cholecystokinin mediates feedback regulation of pancreatic enzyme secretion in rats // Am. J. Physiol. 1986; 250: 252.
- Ihse I., Lilja P., Lundquist I. Feedback regulation of pancreatic enzyme secretion by intestinal trypsin in man // Digestion. 1977; 15: 303.
- Calan J., Bojarski J.C., Spriner C.J. Raw soya-bean flour increases cholecystokinin release in man // Br. J. Nutr. 1987; 58: 175.
- Liener J.E., Goodale R.L., Deshmukh A. et al. Effect of a trypsin inhibitor from soya-beans (Bowman-Birk) on the secretory activity of the human pancreas // Gastroenterology. 1988; 94: 419.
- Owyang C., Louie D., Tatum D. Feedback regulation of pancreatic enzyme secretion // J. Clin. Invest. 1986; 77: 2042.
- Slaff J.I., Jacobson D., Tillman C.R. et al. Protease-specific suppression of pancreatic exocrine secretion // Gastroenterology. 1984; 87: 44.
- Isakson G., Ihse I. Pain reduction by an oral pancreatic enzyme preparation in chronic pancreatitis // Dig. Dis. Sci. 1983; 28: 97–102.
- Lohr J.-M. Exocrine pancreatic insufficiency. Bremen: Int. Med. Publ., 2007; 71.
- Ramo D.J., Puolakkainen P.A., Seppalo K. et al. Self-administration of enzyme substitution in the treatment of exocrine pancreatic insufficiency // Scand. J. Gastroenterol. 1989; 24: 688.
- Halgreen H., Pedersen N.T., Worning H. Symptomatic effect of pancreatic enzyme therapy in patients with chronic pancreatitis // Scand. J. Gastroenterol. 1986; 21: 104.
- Mossner J., Secknus R., Meyer J., Niederau C., Alder G. Treatment of pain with pancreatic extracts in chronic pancreatitis: results of a prospective placebo-controlled multicenter trial // Digestion. 1992; 53: 54.
- Malesci A., Gala E., Fioretta A. et al. No effect of long term treatment with pancreatic extract on recurrent abdominal pain in patients with chronic pancreatitis // Scand. J. Gastroenterol. 1995; 30: 392.
- Маев И.В., Кучерявый Ю.А. Асқазандық қышқыл түзілу және созылмалы панкреатит: байланыс қаншалықты күшті?// Росс. журн. гастроэнтерол., гепатол., колопроктол. 2008; 3: 4–14.
- Белоусова Е.А., Никитина Н.В., Цодиков Г.В. Ферментті препараттармен созылмалы панкреатитті емдеу схемасын оңтайландыру // Фарматека. 2008; 13: 103–108.
- Ивашкин В.Т., Охлобыстин А.В., Баярмаа Н. Созылмалы панкреатит кезінде энтеросолюбильді қабықпен жабылған микрокапсулаланған ферменттердің тиімділігі // Клин. перспект. гастроэнтерол., гепатол. 2001; 5: 15–19.
«Трудный пациент» журналы/ Мұрағат / № 11-2009 / Клиникалық практикадағы панкреатиннің заманауи препараттары